Применение многоатомных спиртов и общая формула по химии
На уроках химии изучают различные определения элементов, веществ и реакции. Многоатомные спирты являются органическими соединениями. В их молекулах содержатся разные гидроксильные группы, которые вступают в реакцию с углеводородным радикалом. По своим свойствам многоатомные спирты имеют похожие качества с одноатомными. Отличие заключается в количестве гидроксильных групп.
Оглавление:
Особенности многоатомных спиртов
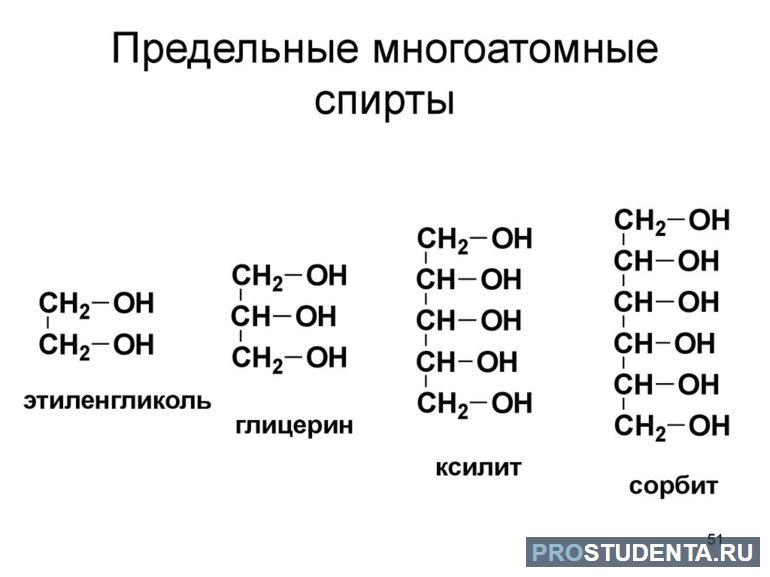
Один из важных представителей многоатомных спиртов — двухатомный этандиол-1,2. Это этиленгликоль. Дополнительно выделяют трёхатомный пропантриол-1,2,3 — глицерин. Отличия заключаются в -ОН в молекулах — изомерия и номенклатура. Эти вещества служат в качестве основных, чтобы создавать другие структурные соединения четырёхатомных и пятиатомных спиртов. Общая формула спирта: CH2OH.
Информация об этиленгликоле
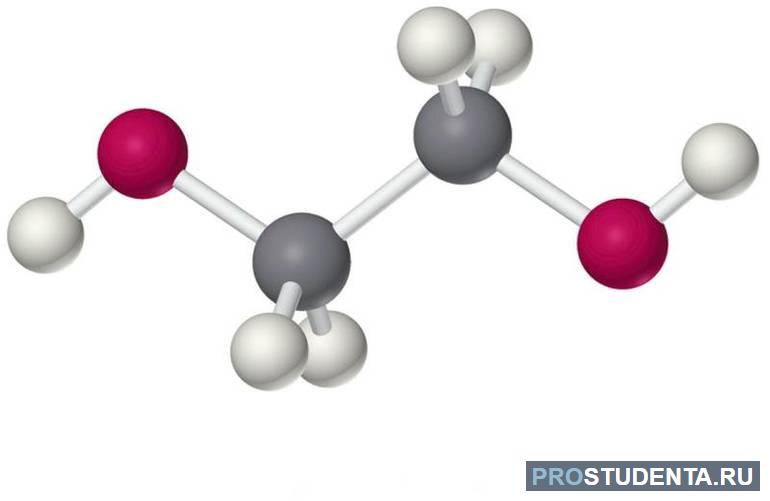
Этиленгликоль является двухатомным спиртом, который не содержит в своём составе примеси. Он полностью прозрачный, его консистенция маслянистая. Если брать другие спирты, этиленгликоль по своим физическим свойствам не имеет специфического и постороннего запаха.
Жидкость обладает сладким вкусом, но к употреблению в пищу запрещена. Если этиленгликоль попадает в организм или на поверхность кожи, появляются повреждения в виде раздражения и ожогов. В медицинской практике есть случаи, когда это соединение приводило к летальному исходу. При внутреннем употреблении в организм попадает повышенное количество токсинов. Этиленгликоль используется в промышленном хозяйстве, продаётся в свободном доступе в специализированных компаниях.
Область применения:
- изготовление топлива для авиационных судов (основная задача заключается в предотвращении обводнения);
- производства взрывчатых веществ на основе нитрогликоля;
- заправка станций, которые занимаются добычей газа в водной среде;
- пропиленгликоль добавляют в крем для обуви, чтобы предотвратить его высыхание при контакте с воздухом.
Это вещество замерзает только при сильном морозе, когда температура воздуха опускается до -65 градусов Цельсия. Соединение имеет свойство самовоспламеняться при определённых условиях. В стандартной окружающей среде вещество полностью безопасное. Отравление организма происходит при регулярном вдыхании паров вещества.
Использование глицерина
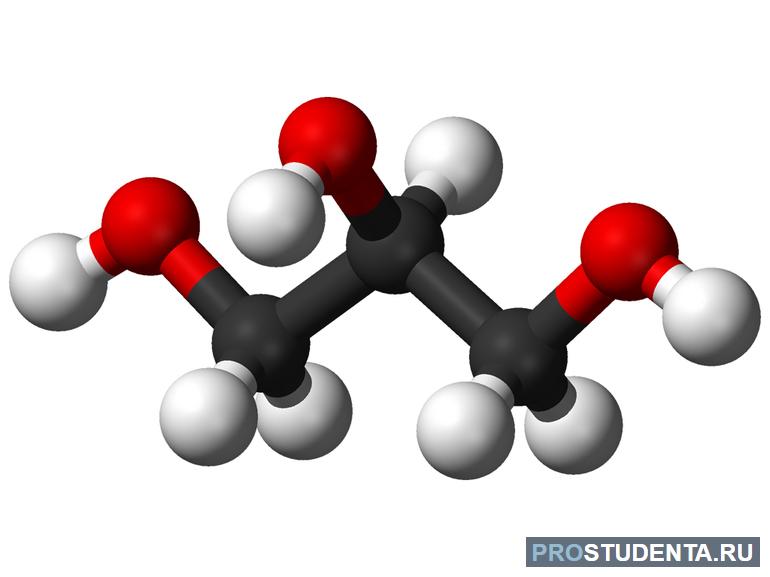
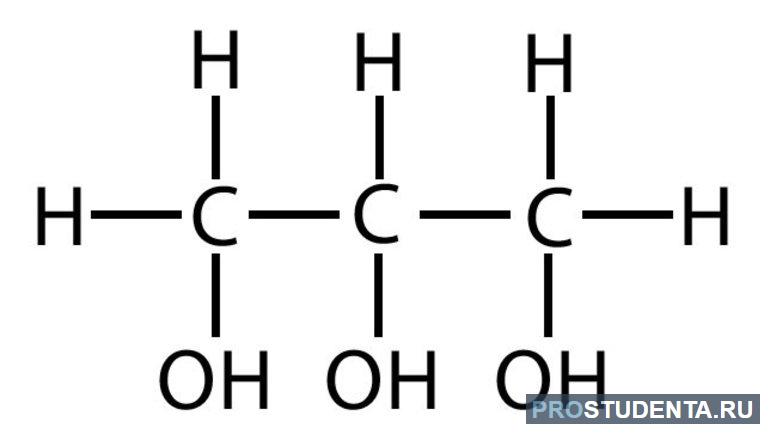
Глицерин является органическим соединением и относится к категории трёхатомных спиртов. Это прозрачная жидкость, которая обладает сладковатым вкусом. Вещество нетоксичное для человека, в отличие от других двухатомных спиртов. Глицерин имеет свойство впитывать влагу из окружающей среды. Его можно смешивать в разных пропорциях с этанолом, ацетоном, метанолом и водой.
Вещество не растворяется в эфире и хлороформе. Когда происходит смешивание, выделяется тепло. Раствор уменьшается в объёме. Глицерин находит применение в пищевой промышленности, в процессе производства табачных изделий, электронных сигарет.
В медицине изготавливают лекарственные препараты. Глицерин добавляют в моющие и косметические средства. Его применяют в промышленности, а также для изготовления пластмассы, лаков и красок, электротехнических деталей. Вещество является хорошим функциональным стабилизатором, который сохраняет и увеличивает предельную степень вязкости.
Как происходит получение
Для получения многоатомных спиртов используют алкены, галогенопроизводные и другие соединения. В промышленности этиленгликоль возникает в результате каталитической гидратации оксида этилена. Когда обрабатывается дигалогенопроизводный водород, происходит появление гликоля. Для этой цели применяют щелочной гидролиз.
В лабораторных условиях применяют окисление алкенов для получения двухатомных спиртов. Этот процесс ещё называют реакцией Вагнера. Для окисления и этерификации алкенов применяют водный или слабощелочной раствор перманганата калия.
Способы получения трёхатомных спиртов:
- В промышленности применяют щелочной гидролиз жиров природного происхождения. Они омыляются, чтобы образовались триглицериды. Процесс гидролиза протекает с применением кислот или щёлочи. Эти вещества выступают в качестве катализатора или при воздействии ферментов — натриевая соль, карбоновая кислота.
- Для кислотного гидролиза животного жира или растительного масла используют глицерилтристеарат в сочетании со стеариновой кислотой для омыления. В результате получается глицерин.
- Использование синтетического способа. Применяют газы крекинга нефти или пропилен. Для получения глицерина не используют пищевое сырьё или жиры растительного происхождения.
Важно соблюдать правильные химические формулы, сочетание пропорций. При получении многоатомных спиртов возникают сложные реакции.
Область применения
Многоатомные спирты находят широкое применение в повседневной жизни. Можно выделить следующие варианты использования:
- Этиленгликоль (HO-CH 2 -CH 2 -OH). Вещество применяется для изготовления лавсана или для производства антифриза. Это водные растворы, которые замерзают при -20 градусах Цельсия. Их применяют для охлаждения двигателя, поэтому транспортное средство эксплуатируется в зимнее время года. Этиленгликоль применяют в качестве сырья при органическом синтезе.
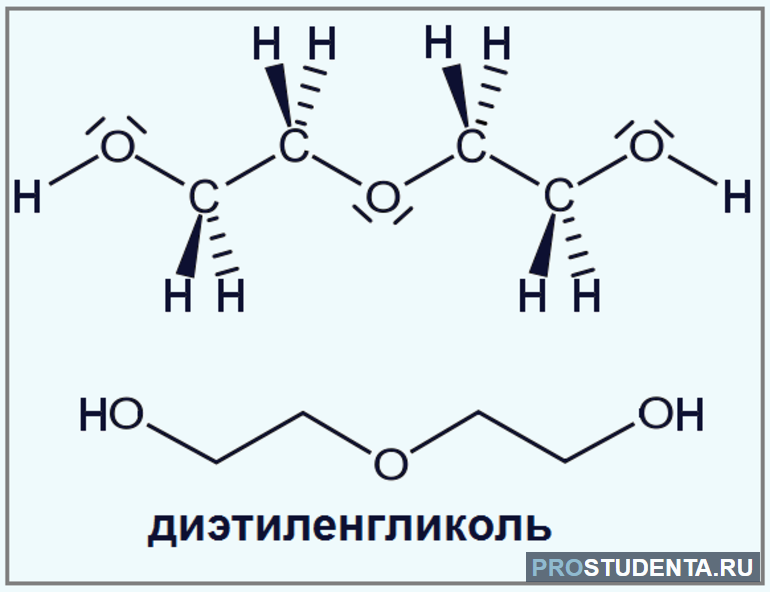
- Диэтиленгликоль (C4H10O3). Его используют для заполнения системы тормозных гидравлических приспособлений. Вещество активно применяется в текстильной промышленности на этапе отделки, придания оттенка ткани.
- Глицерин (C 3 H 5 (OH) 3). Он нашёл широкое применение в разных сферах — парфюмерия, пищевая, текстильная промышленность. Глицерином обрабатывают ткань или кожу, чтобы она сохраняла свои первоначальные свойства.
- Нитроглицерин (C3H5N3O9). Для его производства используют глицерин. Это хорошее сырьё, которое применяют, чтобы получить бездымный порох или динамит. Готовая продукция используется для строительства железных дорог. Нитроглицерин в чистом виде взрывается даже при незначительном ударе, является токсичным веществом. В минимальном количестве — это лекарственное средство для расширения сосудов, улучшения кровоснабжения сердечной мышцы.
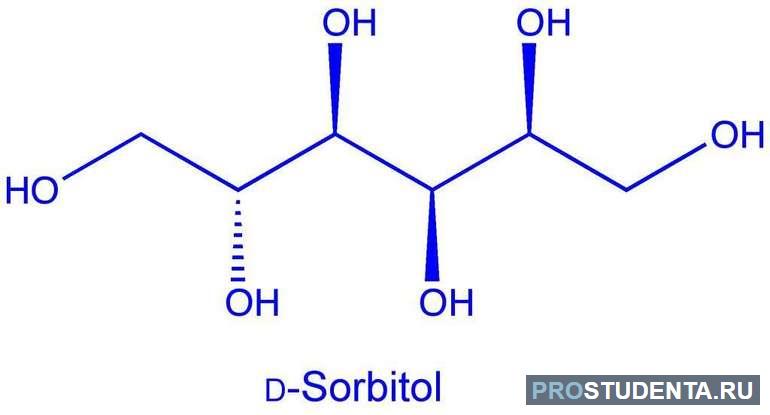
- Сорбит (C 6 H 8 (HO) 6). Его ещё называют глюцитом. Это шестиатомный спирт, который имеет сладкий вкус. Его применяют для изготовления аскорбиновой кислоты. Сорбит — пищевая добавка Е420, которую применяют в качестве заменителя сахара для больных диабетом. Его можно встретить в различных диетических продуктах и напитках.
- Ксилит (CH 2 OH (CHOH) 3 CH 2 OH). Имеет вид сладких кристаллов, которые легко и быстро растворяются при контакте с водой. Применяют для производства продуктов питания людям с сахарным диабетом. Вещество нашло широкое применение при изготовлении олифы, алкидной смолы, поверхностно-активного вещества.
Эти спирты обладают уникальными свойствами. Благодаря этому их применяют в разных сферах промышленности и в бытовых целях.
Общепринятые свойства
Многоатомные спирты являются органическими веществами, поэтому в сочетании углекислого газа и воды они имеют свойство гореть. В результате происходит выделение большого количества тепла. Его применяют в лабораторных условиях для горелок, чтобы проводить опыты и исследования.
Низшие спирты имеют бесцветное пламя, а высшие — жёлтый оттенок, потому что углерод сгорает не полностью. В реакции со щелочным металлом происходит образование алкоголята натрия. По внешнему виду он напоминает обычную соль. Вещество слабой кислоты, легко вступает в гидролиз. Алкоголят неустойчив при сочетании с водой, потому что происходит процесс разложения на щёлочь и спирт.
Спирты не окисляются при контакте с воздухом. Этот процесс происходит в результате нагревания. В качестве примера можно выделить оксид меди, марганцовку, хромовую смесь. В зависимости от строения исходного спирта и воздействия окислителя получаются разные продукты — альдегиды, кетоны. Третичные спирты устойчивы к процессу окисления.
Спирты легко вступают в реакцию, когда используется гидроксид меди. В результате получается прозрачный раствор, который имеет яркий сине-фиолетовый оттенок. Взаимодействие происходит с азотной кислотой.




Ещё никто не комментировал эту статью. Оставьте комментарий первым!